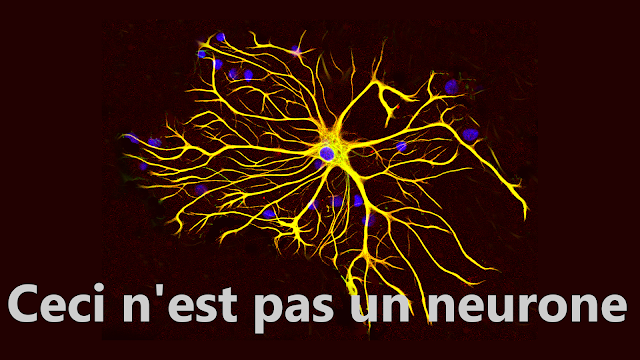
100 milliards de neurones... et bien plus encore.
En 1858, Rudolph Virchow, l’un des grands noms de l’histologie (l’étude des tissus) identifie, au sein des coupes de cerveau qu’il observe, un agglomérat non-identifié qui permet de soutenir les neurones et de maintenir la structure du parenchyme cérébral, qu’il nomme la glie – ou neuroglie. Une quinzaine d’années plus tard, c’est un autre grand nom de la science du vivant, Camilio Golgi, qui s’aperçoit que cette masse informe est en réalité composée de cellules, qui seront nommée en 1891 « Astrocytes » du fait de leur aspect étoilé et extrêmement ramifié.
Au cours du 20ème siècle, différentes théories attribuèrent des rôles distincts aux astrocytes. Certains, comme Golgi, pensent qu’ils servent essentiellement comme soutient aux neurones, qui représentent en quelques sortes les cellules « nobles » du cerveau. Les astrocytes restent dans un rôle subalterne : ils sont chargés d’apporter au neurone le glucose et l’oxygène dont il a besoin pour fonctionner. Cette vision réductrice à été dominante pendant de nombreuses années. Cependant, les dernières décennies de recherche ont considérablement élargi le champs d’action des astrocytes, qui apparaissent aujourd’hui comme des acteurs incontournables du fonctionnement cérébral, et qui pourraient bien supporter les mécanismes les plus fins de notre intelligence.
 |
| Rudolf Virchow (A), Santiago Ramon Y Cajal (B) et Camilio Golgi (C). |
Astrocytes : essentiels à l’éveil…
Alors que l’embryon n’est lové dans le ventre maternel que depuis quelques semaines, certaines cellules de son ébauche cérébrale, les cellules souches neurales, se mettent déjà en action. Rapidement, elles commencent à se diviser pour créer les premiers neurones, encore immatures, qui bientôt partiront vers les lointaines contrées corticales établir leurs colonies.
Un petit peu plus tard, après que les cellules souches neurales aient donné naissance à un nombre démentiel de neurones, se passe un curieux phénomène : les cellules souches arrêtent de produire des neurones, changent de procédés de fabrication et donnent désormais naissance aux astrocytes. Ainsi, en fonction de l’âge de l’échantillon de cerveau que l’on étudie au laboratoire, on pourra observer plutôt une formation de neurones, ou d’astrocytes. Ces deux populations cellulaires ont donc une origine commune !
La production d’astrocytes par les cellules souches neurales reposent aussi sur d’autres mécanismes moléculaires. Par exemple, certains messagers modifient l’accès aux gènes de la cellule souche par des mécanismes épigénétiques : grâce à des modifications chimiques de la molécule d’ADN (méthylation par exemple), ces messagers peuvent « allumer » ou « éteindre » certains gènes capitaux dans l’orientation vers une lignée particulière – neuronale ou astrocytaire.
Ces processus de production sont hautement régulés, par des mécanismes extrêmement complexes qui vont bien au-delà de ce que nous venons de décrire. Par exemple, s’il existe des mécanisme capables de stimuler la production d’astrocytes au détriment des neurones, d’autre ont un effet exactement inverse ! C’est le cas par exemple de la protéine SHP2, dont la mutation est responsable du syndrome de Noonan.
Cette pathologie a été décrite pour la première fois en 1963 par une cardio-pédiatre américaine, Jacqueline Noonan – ce qui n’est pas surprenant car près de 80% des enfants qui souffrent de ce syndrome sont porteur d’une malformation cardiaque. Le syndrome de Noonan, dont la gravité peut beaucoup varier en fonction des patients et des familles, se caractérise aussi par une déformation du visage et du thorax (parfois minime), ainsi qu’un retard des apprentissages chez 30% des malades.
Ce retard intellectuel s’expliquerait par un déséquilibre de formation entre neurones et astrocytes au cours de la vie fœtale. Ainsi, la mutation de SHP2 entrainerait une surproduction de neurones au détriment des astrocytes. Ce déséquilibre déstabiliserait la mise en place des réseaux neuronaux chez le fœtus et perturberait par la suite les acquisitions du jeune enfant.
Un déséquilibre de production neurone/astrocyte se retrouve dans d’autres troubles. C’est le cas par exemple de la trisomie 21, une maladie génétique causée par la présence de 3 chromosomes 21 (au lieu de 2 seulement) dans le génome des patients. Dans leur cerveau, on observe une augmentation des astrocytes et, en miroir, une diminution du nombre de neurones. Certains travaux suggèrent que ces anomalies seraient dues au gène olig2, dont la protéine correspondante stoppe la production neuronale pour favoriser la production astrocytaire. Ce gène étant présent sur le chromosome 21, la copie supplémentaire serait suffisante pour faire basculer la balance.
Un parfait équilibre entre neurone et astrocyte semble donc nécessaire au développement harmonieux du cerveau. Mais la coopération entre ces deux populations de cellules ne se limite pas à la vie intra-utérine. Le rôle des astrocytes semble de nouveau prépondérant dans la mise en place et l’élimination des synapses, les connexions entre deux neurones. Les astrocytes sont par exemple capables de sécréter une protéine appelée thrombospondine, qui stimule la création de synapse. Les souris chez qui ce gène est inactivé possèdent une densité synaptique inférieure à la normale. Après un AVC, la capacité de maintenir et de créer de nouvelles synapses semble liée à la sécrétion de cette protéine par les astrocytes –chez la souris. Les astrocytes pourraient aussi avoir un rôle important dans l’élagage synaptique, un processus d’élimination des synapses inutiles, qui survient grossièrement à l’adolescence.
Même une fois les circuits neuronaux installés et matures, le rôle des astrocytes est essentiel au bon fonctionnement cérébral. Bien sûr, comme nous l’avons déjà évoqué plus haut, ils ont un rôle majeur dans l’apport des nutriments et autres carburants nécessaire au bon fonctionnement neuronal. Le positionnement idéal des astrocytes les prédispose tout particulièrement à ce rôle : ils se trouvent en effet à l’interface entre les vaisseaux sanguins (ils sont l’un des composants de la barrière hémato-encéphalique, une structure complexe séparant de façon quasi-hermétique le cerveau du reste de l’organisme) et les neurones, ce qui leur permet de filtrer le glucose sanguin, de le stocker sous forme de glycogène ou de le transformer en lactate, source d’énergie pour les neurones en action.
Au-delà de l’apport énergétique, les astrocytes interfèrent directement au niveau de la synapse pour permettre une transmission neuronale de qualité. C’est particulièrement le cas pour les synapses excitatrices fonctionnant au glutamate, l’un des principaux neurotransmetteurs du cerveau. Lorsque le neurone en amont (ou pré-synaptique) est dépolarisé par un potentiel d’action, il relargue dans la synapse son neurotransmetteur, qui se fixe alors à la membrane du neurone d’aval (ou post-synaptique), au niveau de récepteurs spécifiques. Cela permet la dépolarisation du neurone post-synaptique et la création d’un nouveau potentiel d’action.
L’astrocyte est aussi capable de synthétiser par lui-même du glutamate et alimente donc le neurone en neurotransmetteur. Mais il peut aussi synthétiser d’autres substances qui ont une action essentielle dans l’apprentissage et la mémoire, comme la sérine.
Au niveau des synapses, le glutamate peut se lier à différents types de récepteurs, dont le plus classique est l’AMPA-R, dont l’activation entraîne la dépolarisation du neurone post-synaptique. Mais il existe aussi un autre type, appelé NMDA-R, dont le fonctionnement est légèrement différent. En effet, pour que ce canal puisse s’ouvrir, il nécessite non seulement la liaison du glutamate, mais aussi une dépolarisation du neurone (provoquée par la stimulation de l’AMPA-R) et la liaison d’un autre neurotransmetteur, la sérine. Une fois ouvert, le NMDA-R permettra l’entrée d’ion calcium, ce qui permettra, par le biais de nombreux mécanismes cellulaires, l’intégration d’un nombre plus important d’AMPA-R à la surface du neurone, et donc un renforcement de la synapse. L’action conjointe des AMPA-R et des NMDA-R correspond à l’un des mécanismes principaux de la plasticité synaptique. Pendant longtemps, on pensait que la sérine provenait uniquement des neurones pré-synaptiques. Mais des travaux de recherche ont mis en évidence une origine astrocytaire importante : ainsi, lorsqu’on empêche la libération de sérine spécifiquement par les astrocytes, on limite drastiquement la plasticité synaptique !
Ce phénomène repose pour beaucoup sur des interneurones inhibiteurs, sensibles à la dépolarisation du neurone central et qui se projettent sur les synapses adjacentes. Ainsi, lorsque la synapse centrale tétanise, les interneurones envoient un puissant signal inhibiteur aux synapses voisines.
On s’est cependant aperçu qu’encore une fois, les astrocytes avaient leur mot à dire dans ce phénomène. En effet, en réponse à la tétanie centrale, ils sécrètent de l’adénosine, une molécule impliquée notamment dans le sommeil et capable d’inhiber les synapses excitatrices.
Les interactions entre neurones et astrocytes, au cours de la vie fœtale, du cerveau en développement comme chez l’adulte, sont extrêmement complexes et sont l’objet d’une recherche riche et passionnante. Ces travaux de pointe nous ont permis d’étendre, et parfois de contredire, les vieilles théories des premiers explorateurs de notre système nerveux. Cependant, nous allons voir que ces pionniers ont parfois eu une intuition déroutante.
… comme au sommeil.
Ramon y Cajal, un scientifique espagnol, est l’un des plus brillant esprit qui s’est penché sur le fonctionnement de notre cerveau. Au début du XXème siècle, il étudia ces cellules toutes nouvellement découvertes et nommées, les astrocytes. Il décrivit avec brio les longs prolongements cellulaires qui traversent le parenchyme cérébral et qui s’enroulent autour des synapses. Ses descriptions sont d’une précision incroyable pour l’époque. Il nomma, suite à ses observations, une théorie étrange sur le rôle des astrocytes : ils seraient capables d’induire le sommeil grâce à leurs prolongements près des synapses, qui se rétracteraient en journée pour permettre l’éveil. Les astrocytes permettraient, la nuit, d’inhiber le fonctionnement des neurones et favoriseraient ainsi le sommeil.
Cette théorie farfelue n’eut aucune validation scientifique… jusqu’en 2005. Cette année-là, une souris génétiquement modifiée pour empêcher le bon fonctionnement des astrocytes fut créée. La mutation en question bloquait tout mécanisme d’excrétion de l’astrocyte –plus précisément, un phénomène appelé exocytose, une excrétion de molécules contenues dans une vésicule à l’intérieur de la cellule et qui est extériorisée.
Les premières expériences aboutirent à des résultats surprenants. Chez ces souris, l’intensité de la transmission synaptique était drastiquement augmentée ! Au vue de l’importance des astrocytes dans le fonctionnement de la synapse, cela a quelque chose de surprenant ! Rapidement, les scientifiques découvrirent que les astrocytes génétiquement modifiés étaient surtout incapable de sécréter de l’adénosine, une molécule connue pour son implication dans la régulation du sommeil.
En effet, l’adénosine est un puissant inducteur du sommeil. Si votre café ou votre Red Bull vous permet de rester éveillé, c’est parce que la caféine qu’il contiennent représente un inhibiteur efficace de l’adénosine !
Au niveau de la synapse, l’action de l’adénosine est complexe. Comme nous l’avons vu précédemment, elle peut inhiber la transmission synaptique, lorsqu’elle se fixe sur son récepteur au niveau du neurone pré-synaptique. Mais elle peut aussi favoriser la plasticité synaptique en se fixant sur son récepteur post-synaptique, car elle permet le maintien des NMDA-R à ce niveau. Ainsi, chez nos souris aux astrocytes défaillants et privées d’adénosine, la transmission synaptique se majore, mais le nombre de NMDA-R post-synaptique chute, aboutissant à une diminution de la plasticité. Au niveau fonctionnel et comportemental, ces souris ne présentent pas de réduction du temps de sommeil mais ce dernier semble perturbé, comme en atteste les mesures du fonctionnement cérébral par électro-encéphalographie.
L’action des astrocytes sur la régulation du sommeil est encore imparfaitement comprise. Mais leur action semble substantielle. Ces découvertes ouvrent la porte à de nouvelles approches (et traitements) des troubles du sommeil, qui caractérisent de nombreuses pathologies. Nous agissons actuellement exclusivement sur les neurones, mais les astrocytes pourraient représenter un levier intéressant pour soulager ces malades !
Les astrocytes représentent une population cellulaire majeure de notre cerveau. Chacun d’entre eux est connecté à près de 2 millions de synapses. Leur action ne peut être limitée au simple rôle de support métabolique de messeigneurs neurones. Ils sont impliqués dans la formation des circuits neuronaux, au bon fonctionnement des synapses et même dans la régulation du sommeil ! Ils font partie intégrante de notre cerveau et participent pleinement aux capacités propres aux Hommes.
SOURCES :
- https://www.orpha.net/data/patho/Pub/fr/Noonan-FRfrPub206.pdf
- https://en.wikipedia.org/wiki/Noonan_syndrome#History
- https://fr.wikipedia.org/wiki/R%C3%A9cepteur_NMDA
- Haydon, Philip G. "Astrocytes and the modulation of sleep." Current opinion in neurobiology 44 (2017): 28-33.
- Sloan, Steven A., and Ben A. Barres. "Mechanisms of astrocyte development and their contributions to neurodevelopmental disorders." Current opinion in neurobiology 27 (2014): 75-81.
- Parpura, Vladimir, et al. "Glial cells in (patho) physiology." Journal of neurochemistry 121.1 (2012): 4-27.
CREDITS PHOTOS :
Par Auteur inconnu — http://ihm.nlm.nih.gov/images/B29494, Domaine public, https://commons.wikimedia.org/w/index.php?curid=138415
By Unknown author - [1] [2] [3], Public Domain, https://commons.wikimedia.org/w/index.php?curid=10308907
Par Original photo is anonymous although published by Clark University in 1899. Restoration by Garrondo — Cajal.PNG, Domaine public, https://commons.wikimedia.org/w/index.php?curid=12334552
Image par Clker-Free-Vector-Images de Pixabay
Image par OpenClipart-Vectors de Pixabay
Image par OpenClipart-Vectors de Pixabay
Par Henry Vandyke Carter — Henry Gray (1918) Anatomy of the Human Body (See "Livre" section below)Bartleby.com: Gray's Anatomy, Planche 623, Domaine public, https://commons.wikimedia.org/w/index.php?curid=541442
Par JDifool — Travail personnel, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=4470995
By GerryShaw - Own work, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=29369565
Image par Venita Oberholster de Pixabay
By en:User:Diberri - Own work, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=1918091
By RicHard-59 - Own work, based on File:Activated NMDAR.PNG, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=21286587
Par vectorization: Mouagip (talk)Synapse_diag1.png: Drawn by fr:Utilisateur:DakeCorrections of original PNG by en:User:NretsCette image vectorielle non W3C-spécifiée a été créée avec Adobe Illustrator. — Synapse_diag1.png, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=11438067
By Tomwsulcer - Own work, CC0, https://commons.wikimedia.org/w/index.php?curid=1550951